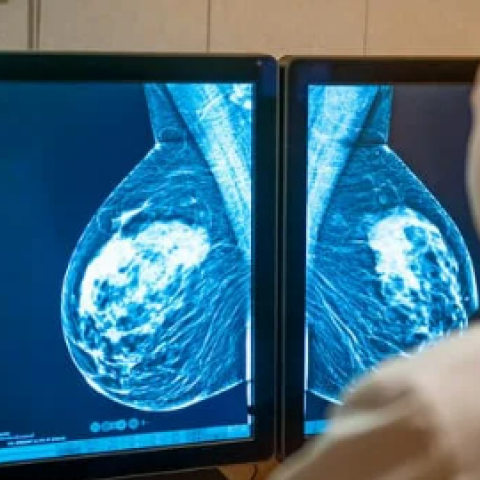
IA et dépistage du cancer du sein - Quelles pistes ?
Dans une étude publiée récemment1, une équipe allemande propose une stratégie originale d’intégration de l’intelligence artificielle (IA) au dépistage organisé du cancer du sein, avec en point de mire deux objectifs : classer rapidement et avec un haut degré de confiance des mammographies normales (triage), tout en améliorant la détection des cancers.
L’utilisation de l’IA dans le dépistage du cancer du sein présage à la fois d’immenses opportunités mais également de défis majeurs, dont les déclarations médiatiques ne se font que rarement l’écho. En plus des performances diagnostiques « intrinsèques » de l’IA, son utilisation et son positionnement dans la chaîne du dépistage en double lecture2 vont directement influer sur son impact clinique et sociétal, positif ou négatif, et sur le niveau de confiance apporté au dépistage organisé.
En effet, l’utilisation d’un système d’aide au diagnostic par l’IA peut se faire au moment de l’interprétation, ce qui permet d’améliorer la sensibilité de détection tumorale, mais risque également d’augmenter les faux positifs, et n’offre pas de réponse aux contraintes croissantes sur les ressources radiologiques. A contrario, l’utilisation de l’IA autonome ou en premier lecteur (triage) peut soulager la charge de travail du radiologue, mais également potentiellement dégrader la sensibilité du dépistage.
La stratégie proposée par Leibig et al. combine un triage initial des clichés classés normaux par l’IA avec un haut degré de certitude, un rôle central du radiologue pour les cas incertains ou pathologiques et un « filet de sécurité » permettant à l’IA de « rattraper » des cancers non vus.
Cette stratégie combinée est évaluée rétrospectivement, et comparée à la lecture humaine non aidée et à l’IA autonome. Le modèle d’IA a été élaboré à partir d’une large base de données, multiconstructeur, représentative du dépistage organisé.
La performance évaluée de l’IA autonome (sensibilité 84,6% [83,3-85,9] et spécificité 91,3% [91,1–91,5]) était inférieure à celle d’un radiologue non aidé (sensibilité 85,7% et spécificité 93,4%), elle-même inférieure à la stratégie combinée IA + radiologue (sensibilité 89,7%, spécificité 93,8%). La stratégie combinée permettait également de trier automatiquement 63% des examens.
Les résultats très encourageants de cette étude confortent donc les stratégies de partenariat IA-radiologue, permettant d’automatiser certaines tâches tout en maintenant / améliorant la qualité et la sécurité du dépistage, à l’exact opposé du remplacement d’un des lecteurs par l’IA. Parmi les limites de l’étude, notons l’absence de prise en compte de la manière dont les recommandations de l’IA influencent la décision des radiologues « dans la vrai vie ». Enfin, il faut considérer ce type d’étude comme des « preuves de concept » plus que des solutions immédiatement implémentables, étant donné la diversité importantes (en conception et performances) des outils d’IA disponibles sur nos consoles.
1. Combining the strengths of radiologists and AI for breast cancer screening : a retrospective analysis, C.Leibig, M.Brehmer, S.Bunk, D.Byng, K.Pinker, L.Umutlu, The Lancet Digital Health, July 2022
2. Double lecture indépendante avec évaluation des discordances en consensus ou par arbitrage (système germanique et scandinave), double lecture des examens classés normaux par le premier lecteur (système français).
Sébastien Molière, Imagerie B, CHU de Strasbourg