FFR-IA pour la détection de sténoses coronaires significatives en comparaison au scanner de perfusion myocardique
Le scanner de perfusion myocardique couplé au coroscanner allie l’étude de l’anatomie des coronaires avec une analyse fonctionnelle au prix d’une dose d’exposition et de produit de contraste supplémentaires. D’autres part, la FFR-CT basée sur la dynamique de flux virtuelle, permet de modéliser un arbre coronaire à partir de données de coroscanner. Cependant cette technique nécessite actuellement un traitement de données hors site dans un laboratoire centralisé. De plus, elle n’est pas remboursée en France. Cependant, de nouvelles techniques de FFR-CT basées sur le deep learning offrent le potentiel d’une utilisation rapide et locale.
L’objectif de cette étude était d’évaluer les performances diagnostiques d’un logiciel de FFR-CT basé sur du deep learning (FFR-IA) dans la détection de sténoses hémodynamiquement significatives en comparaison au scanner de perfusion myocardique.
Dans cette étude rétrospective, nous avons inclus 100 patients ayant bénéficié d’un coroscanner et d’un scanner de perfusion myocardique dynamique (MPI-CT) sur un scanner double source de troisième génération (SOMATOM Force, Siemens Healthineers) du 1er aout 2023 au 31 janvier 2024. Dans notre centre, le MPI-CT au regadenoson est réalisé chez les patients présentant soit un score calcique ≥ 300, soit une sténose coronaire maximale ≥50% (CAD-RADS ≥ 3), soit en présence de stent coronaire. Les cartographies de perfusion myocardique étaient interprétées par deux radiologues. Un défect de perfusion était identifié par une diminution du débit sanguin myocardique (MBF) détecté visuellement dans un territoire coronaire systématisé (après un fenêtrage à 100 mL/100 mL/min par défaut). Le défect était confirmé si le rapport MBF myocarde pathologique / myocarde sain était ≤ 0,7. Une acquisition au temps tardif 5 minutes après injection de produit de contraste a été systématiquement réalisée pour exclure la présence de séquelles d’infarctus. Une ischémie myocardique était par conséquent définie par la présence d’un défect de perfusion en l’absence de séquelle d’infarctus dans le même territoire. Des reconstructions curvilignes multiplanaires des artères coronaires étudiées étaient exportées dans le logiciel CorEx (Spimed-AI, version 2.0), qui classifiait chaque artère en FFR ≤ 0,8 ou FFR > 0,8.
Sur 100 patients, un ou plusieurs défects étaient visualisés chez 41 patients. En comparaison au MPI-CT et en analyse per-patient, la FFR-IA avait une sensibilité, spécificité, VPP, VPN et une précision diagnostique de 98%, 31%, 49%, 95% et 58%, respectivement. Dans le sous-groupe des patients non stentés, ces valeurs étaient de 95%, 39%, 45%, 94% et 59%, respectivement.
En analyse per-vaisseau, la FFR-IA avait une sensibilité, spécificité, VPP, VPN et précision diagnostique de 90%, 61%, 35%, 96% et 67%, respectivement. Dans le sous-groupe non stenté, ces valeurs étaient de 84%, 76%, 40%, 96% et 77%, respectivement. Dans notre population, la FFR-IA aurait évité la réalisation de 18 scanners de perfusion myocardique (18%).
En comparaison avec le MPI-CT, la FFR-IA montre une très bonne sensibilité et VPN pour l’identification de sténose coronaire hémodynamiquement significative. La FFR-IA montre ainsi le potentiel d’une utilisation comme filtre avant la réalisation d’un scanner de perfusion myocardique en coroscanner.
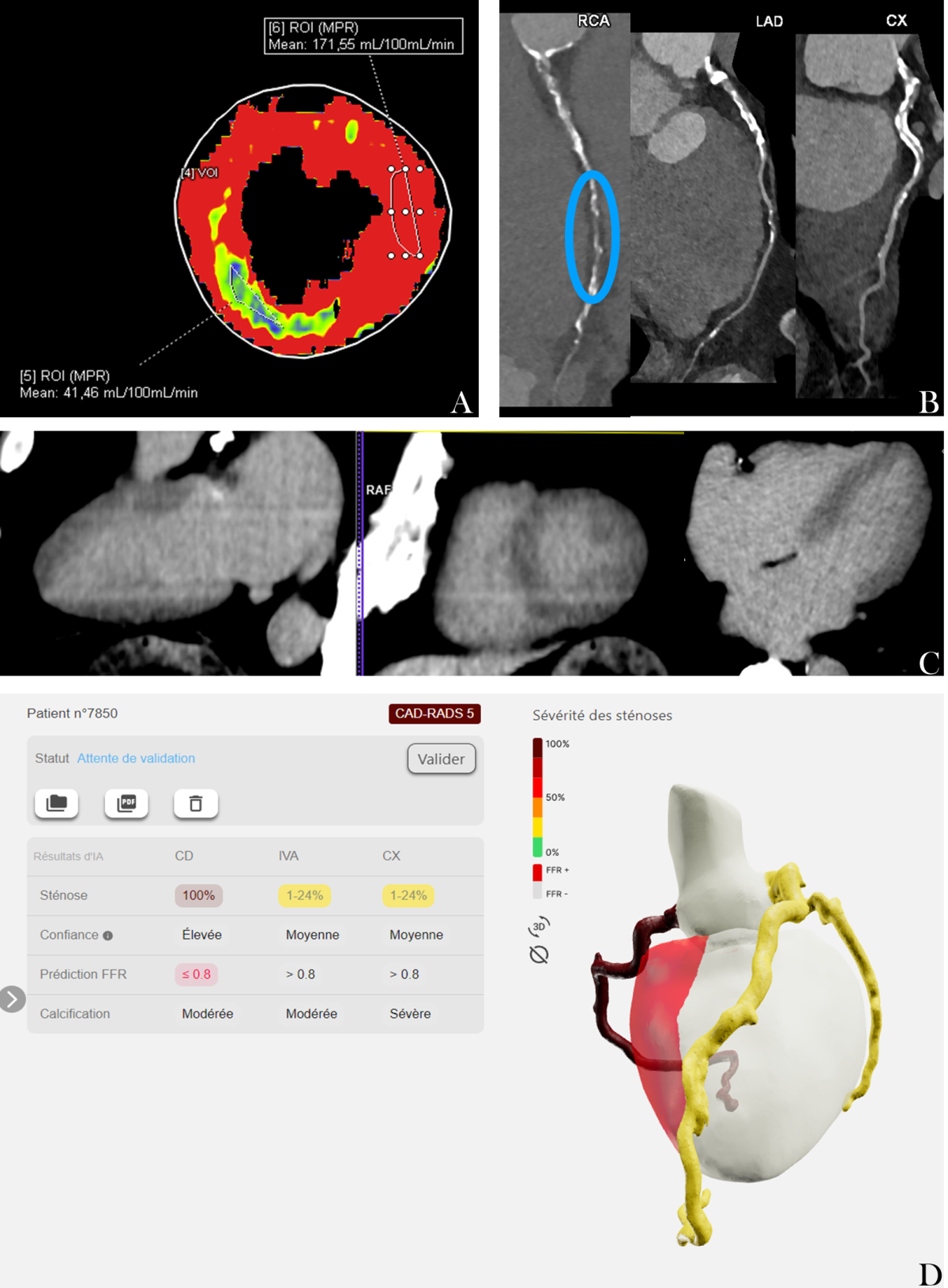
Scanner de perfusion myocardique (A) chez un patient ayant présenté des douleurs thoraciques à l’effort depuis 2 mois, avec un défect de perfusion significatif dans le territoire inférieur du myocarde et une occlusion de l’artère coronaire droite (B), sans séquelle d’infarctus au temps tardif (C), avec une FFR-IA ≤ 0,8 sur l’artère coronaire droite (D).
